Aidez-moi à trouver le DAE qui me convient
Répondez à quelques questions et nous vous indiquerons l’appareil qui répond le mieux à vos besoins.
Dites-nous en plus sur vous





Où et comment ce défibrillateur automatisé externe (DAE) sera-t-il utilisé ?



Où et comment ce défibrillateur automatisé externe (DAE) sera-t-il utilisé ?


Où et comment ce défibrillateur automatisé externe (DAE) sera-t-il utilisé ?


Où et comment ce défibrillateur automatisé externe (DAE) sera-t-il utilisé ?


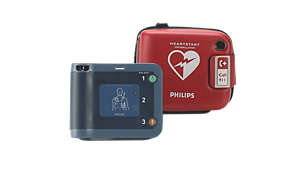
D'après la profession que vous avez indiquée, nous vous recommandons le défibrillateur automatisé externe HeartStart FRx. Ce modèle, bien qu'utilisable par toute personne même non formée, est particulièrement adapté aux utilisateurs disposant d’une formation de base, comme les infirmières scolaires, les professionnels de santé, les ambulanciers, les pompiers ou encore la police. Le FRx est conçu pour être utilisé dans environnements contraignants, y compris en extérieur, sur des chantiers de construction ou dans des véhicules, des avions, des hélicoptères ou encore des bateaux. Ses atouts:
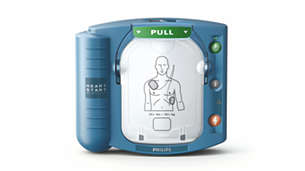
D'après votre réponse, nous vous recommandons le défibrillateur automatisé externe HeartStart HS1 Grand Public. Il est spécialement conçu pour les bureaux, les bibliothèques, les salles de sport et tous les espaces publics où les utilisateurs ne bénéficient pas forcément d’une formation clinique et/ou médicale. Ses atouts: