mai 16, 2023
Philips publie les derniers résultats du programme complet des tests et essais effectués pour les appareils de traitement du sommeil par PPC et BiPAP.
Amsterdam, Pays-Bas - Royal Philips (NYSE : PHG ; AEX : PHIA) publie aujourd'hui les nouveaux résultats du programme complet de tests et essais de sa filiale Philips Respironics afin de mieux évaluer la nature des risques potentiels liés à la mousse d'insonorisation en polyuréthane à base de polyester (PE-PUR) utilisée dans certains appareils de PPC, BiPAP et ventilateurs mixtes dans le cadre de la notification de sécurité émise en Juin 2021.
Les évaluations du risque sont désormais finalisées pour les appareils de traitement du sommeil par PCC et BiPAP concernés par la notification de sécurité, c'est à dire les DreamStation de première génération, les System One et DreamStation Go, représentant environ 95% des appareils enregistrés au total.
Les évaluations s'appuient également sur les précédents rapports de décembre 2021, juin 2022 et décembre 2022. En outre, des tests et des analyses ont été réalisés pour les appareils DreamStation de première génération qui ont été exposés au nettoyage à l'ozone.
Méthodes de test
Le programme de tests et essais a été conduit en collaboration avec cinq laboratoires d'essais indépendants et certifiés, et les résultats ont été revus et évalués par des experts tiers qualifiés indépendants, par Philips Respironics ainsi que par un panel médical externe indépendant.
Les méthodes d’essais appliquées - comprenant planification des essais, exécution des tests et interprétation des résultats pour une évaluation complète des risques - sont conformes aux normes industrielles ISO 18562 [1,2] et ISO 10993 [3] applicables. La méthodologie d'essai appliquée a été scientifiquement étayée sur la base d'un examen approfondi et d'une atténuation des limites inhérentes à toute norme d'essai et/ou recherche scientifique. Par exemple, les tests ont été effectués sur plusieurs appareils usagés, avec différentes durées d'utilisation par les patients et différents degrés de dégradation visuelle de la mousse, ainsi que sur des mousses vieillies en laboratoire, volontairement dégradées à différents niveaux. D'autres exemples sont fournis à la fin de ce communiqué de presse.
"Notre priorité absolue est la santé et le bien-être des patients ", a déclaré Roy Jakobs, PDG de Royal Philips.
Résultats pour les appareils de traitement du sommeil non exposés au nettoyage à l'ozone
Les résultats du programme complet de tests et essais pour les appareils DreamStation de première génération, System One et DreamStation Go indiquent que l’exposition potentielle des patients aux émissions de matières particulaires (MP) et composés organiques volatils (COV) provenant de la mousse PE-PUR de ces dispositifs, est peu susceptible d’entrainer un préjudice significatif pour la santé des patients. Les tests effectués et les conclusions sont résumés dans le tableau ci-dessous.
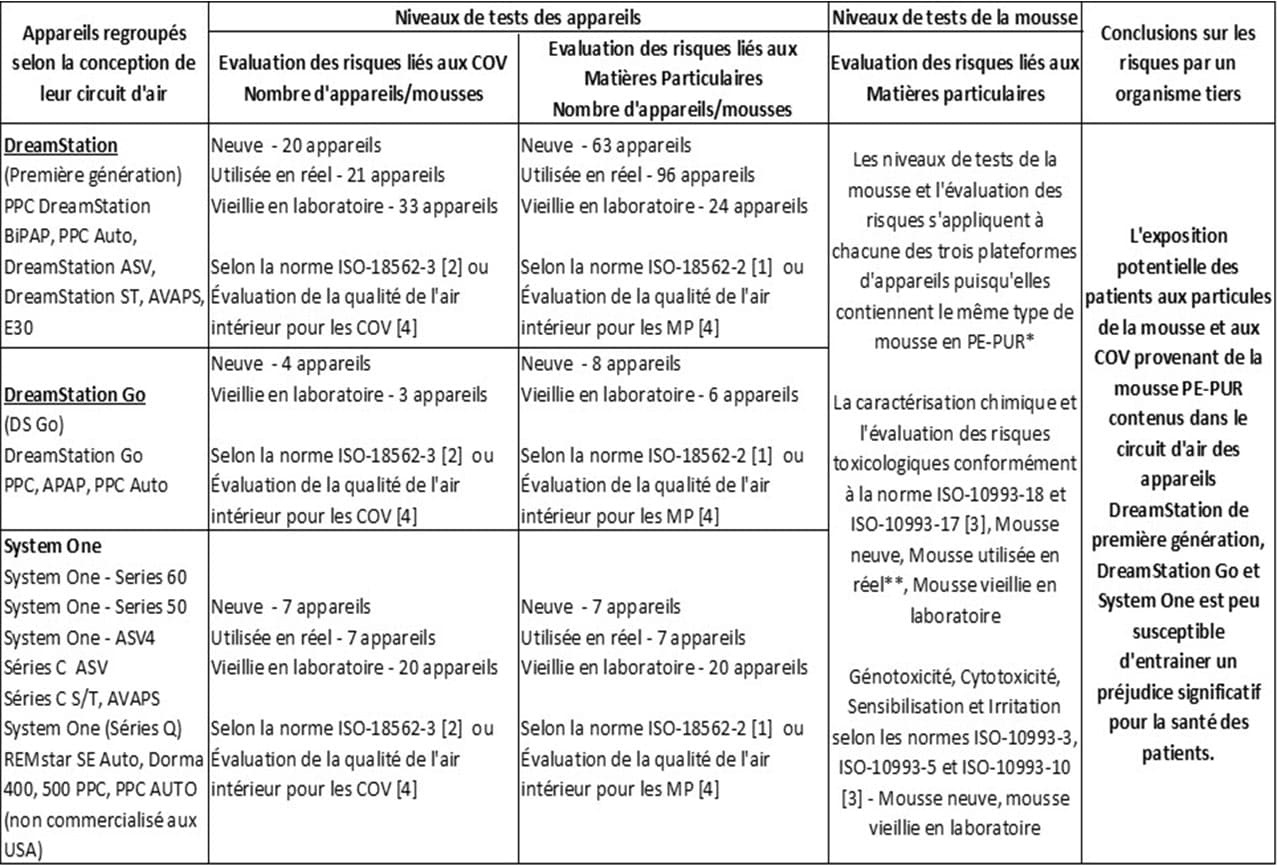
COV: Composés Organiques volatils ** La mousse de 7 appareils différents de DreamStation, de première génération, utilisés en réel a été caractérisée chimiquement conformément à la norme ISO 10993-18 et -17 [3] et comprenait des mousses dans différents états de dégradation visuelle de façon représentative
MP: Matières Particulaires
*La quantité totale de mousse dans les appareils varie d'environ 1 g à 10 g, en fonction de la conception et de la configuration du circuit d’air de l'appareil. Les dispositifs de chacune des plateformes ont la même conception et configuration du circuit d’air, y compris la quantité de mousse présente.
Des tests plus poussés et des évaluations des risques toxicologiques sur plusieurs dispositifs avec une mousse neuve, utilisée « en réel » et vieillie en laboratoire montrent qu'il n'y a pas de danger pour la santé concernant les COV détectés sur la base des tests et essais de la norme ISO 18562-3 [2]. En outre, une évaluation des risques réalisée par des experts tiers conclue qu'il est peu probable que l’exposition aux COV pour ces dispositifs entraine un préjudice significatif pour la santé des patients.
Des dispositifs neufs, vieillis en laboratoire et utilisés en réel ont été testés et tous étaient conformes aux critères d’acceptation de la norme ISO 18562-2 [1] pour les émissions de MP. Les tests ont été effectués sur des dispositifs utilisés en réel (c'est à dire des appareils précédemment utilisés par des patients) présentant différents degrés de dégradation (c'est-à-dire de l'absence de dégradation visible à une dégradation visible sévère), sur des dispositifs neufs et sur des dispositifs avec de la mousse vieillie en laboratoire qui avait été exposée intentionnellement à des températures (≥80°C) et à une humidité (≥75% HR) significativement élevées pour accélérer la dégradation.
En outre, les émissions de MP testées des dispositifs utilisés en réel présentant une dégradation de la mousse n'étaient pas statistiquement différentes des émissions de MP des dispositifs utilisés en réel sans dégradation, ce qui suggère que la dégradation n'a pas contribué à des niveaux élevés de particules respirables dans les appareils testés.
Même en partant de l'hypothèse très prudente et théorique que l’ensemble de la mousse PE-PUR pourrait se dégrader et qu’un patient serait alors exposé à toute la mousse PE-PUR dégradée contenue dans le dispositif, l'évaluation des risques réalisée par un organisme tiers a conclu qu'il est peu probable que l'exposition aux particules provenant de la mousse dégradée de ces dispositifs, y compris les particules respirables et non respirables potentielles, entraîne un préjudice significatif pour la santé des patients.
Sur la base de l'inspection visuelle de la mousse des appareils DreamStation de première génération retournés, la fréquence de la dégradation visible de la mousse s'est avérée faible. L'inspection visuelle ne permet d'identifier que la dégradation visible de la mousse et ne peut pas mesurer la production de composés organiques volatils ou quantifier la perte de particules, c'est pourquoi des tests et des analyses supplémentaires ont été effectués comme décrit ci-dessus et dans la publication complète.
III - L'impact du nettoyage à l'ozone sur la dégradation de la mousse PE-PUR sur les appareils DreamStation de première génération
Philips Respironics a finalisé les tests et essais pour les modèles d’appareils DreamStation de première génération exposés au nettoyage à l’ozone :
Résumé des tests en cours
Philips Respironics est en train d'achever divers autres tests et analyses restants. Les évaluations du risque pour les appareils System/PR One et DreamStation Go (contenant la même mousse que les appareils DreamStation de première génération) exposés au nettoyage à l’ozone ont été finalisées. Pour les ventilateurs Trilogy 100/200 et Omnilab Advanced Plus, les tests sur les COV et particules se poursuivent, ainsi que l’évaluation chimique et l’évaluation des risques toxicologiques. Ces appareils contiennent un type de mousse PE-PUR différent de celui des appareils DreamStation de première génération. Philips Respironics prévoit de fournir une mise à jour de ces tests au troisième trimestre 2023.
Recommandations aux prestataires de santé et aux patients
Il est demandé aux patients utilisant un appareil de PCC ou BiPAP qui n’a pas encore été remplacé ni enregistré, de le faire enregistrer afin de faciliter son remplacement.
Philips Respironics continue de conseiller aux patients utilisant les appareils de PPC ou BiPAP concernés qui n’ont pas été remplacés, de contacter leur médecin ou leur prestataire de santé à domicile pour décider d'un traitement adapté à leur situation, qui peut inclure l'arrêt de l'utilisation de leur appareil, la poursuite de l'utilisation de l'appareil concerné, l'utilisation d'un autre appareil similaire ne faisant pas l'objet d’une notification de sécurité ou le recours à des traitements alternatifs du syndrome d’apnées du sommeil. En outre, il est conseillé aux patients de suivre les instructions et les recommandations de Philips Respironics concernant le nettoyage et le remplacement de leur appareil et de ses accessoires. Le nettoyage à l'ozone et à la lumière UV ne sont pas des méthodes de nettoyage actuellement approuvées pour les appareils ou les masques et ne doivent pas être utilisées.
Philips Respironics recommande également aux utilisateurs de ventilateurs à domicile de contacter leurs prestataires de santé à domicile avant d'apporter des modifications à leur traitement.
Fondement scientifique des méthodes d'essais
La méthodologie d’essai appliquée a été scientifiquement étayée sur la base d'un examen approfondi et d'une atténuation des limites de tests inhérentes à toute norme d’essai et/ou recherche scientifique. Pour illustrer cela, des exemples de ces considérations et atténuations ont été énumérés ci-dessous.
Le fondement scientifique des méthodes d’essais appliquées comprenait un examen approfondi et une réduction des limites des essais, par exemple :
Notes [2] ISO 18562-3 : Évaluation de la biocompatibilité des voies de gaz respiratoires dans les applications de soins de santé - Partie 3 : Essais concernant les émissions de composés organiques volatils (COV). [3] ISO 10993 : Évaluation biologique des dispositifs médicaux ; Partie 1 : Évaluation et essais au sein d’un processus de gestion du risque ; Partie 3 : Essais concernant la génotoxicité, la cancérogénicité et la toxicité sur la reproduction ; Partie 5 : Essais concernant la cytotoxicité in vitro ; Partie 10 : Essais d'irritation et de sensibilisation cutanée ; Partie 17 : Établissement des limites admissibles des substances relargables ; Partie 18 : Caractérisation chimique des matériaux des dispositifs médicaux dans le cadre d'un processus de gestion du risque. [4] La norme utilisée pour les essais avant la norme ISO 18562. [5] Les appareils DreamStation, SystemOne et DreamStation Go de première génération contiennent de la mousse PE-PUR de type A, tandis que les appareils Trilogy 100/200 contiennent de la mousse PE-PUR de type B et les appareils OmniLab Advanced Plus contiennent des mousses PE-PUR de type A et B. Les différences connues entre les mousses de type A et de type B sont que la mousse de type B peut être utilisée avec un adhésif acrylique sensible à la pression, qu'elle a une densité plus faible, une épaisseur différente et qu'elle contient également un additif pour réduire l'inflammabilité potentielle.
*Il s’agit d’une notification de rappel pour les États-Unis uniquement, et d’une notification de sécurité assortie d’une action corrective pour la France notamment.
[1] ISO 18562-2 : Évaluation de la biocompatibilité des voies de gaz respiratoires dans les applications de soins de santé - Partie 2 : Essais concernant les émissions de matières particulaires.
A propos de Royal Philips
Royal Philips (NYSE: PHG, AEX: PHIA) est une entreprise leader en technologies médicales dont la mission principale est d’améliorer la santé des personnes au travers de solutions et services autour du Continuum de soin : Mode de vie sain, Prévention, Diagnostic, Traitement et Soins à domicile. Philips utilise des technologies de pointe et s’appuie sur les retours cliniques et les consommateurs pour concevoir des solutions intégrées. Basé aux Pays-Bas, l'entreprise est leader dans l'imagerie diagnostique, la thérapie guidée par imagerie, le monitorage patient et l'informatique clinique, ainsi que dans le bien-être, la santé personnelle et les soins à domicile. Philips a réalisé, avec son portefeuille de solutions Santé et Bien-être, un chiffre d’affaires de 17,2 milliards d'Euros en 2021, emploie environ 78 000 salariés et propose ses produits et services dans plus de 100 pays». Les informations sur Philips sont disponibles sur: www.philips.com/newscenter (en anglais)
Déclarations prospectives
Cette déclaration contient certaines déclarations prospectives concernant la situation financière, les résultats d'exploitation et les activités de Philips et certains des plans et objectifs de Philips concernant ces éléments. Des exemples de déclarations prospectives comprennent les déclarations faites sur la stratégie, les estimations de la croissance des ventes, l'EBITA futur, les développements futurs de l'activité organique de Philips et la réalisation des acquisitions et des cessions. De par leur nature, ces déclarations impliquent des risques et des incertitudes car elles se rapportent à des événements et circonstances futurs et de nombreux facteurs pourraient faire en sorte que les résultats et développements réels diffèrent sensiblement de ceux exprimés ou sous-entendus par ces déclarations.
Topics
Contacts

Steve Klink
Philips Global Press Office Tel: +31 6 10888824
You are about to visit a Philips global content page
Continue
Elco van Groningen
Philips Global Press Office Tel: +31 6 8103 9584
You are about to visit a Philips global content page
ContinueMedia assets
Press releases
Get our press releases by e-mail
You are about to visit a Philips global content page
Continue